成都生物所發(fā)現(xiàn)新型化學(xué)小分子藥物靶向TRBP-Dicer蛋白相互作用調(diào)節(jié)microRNA生物合成治療肝癌的研究成果
作者:王飛
時間:2022-08-26
近日,中國科學(xué)院成都生物研究所王飛研究員團(tuán)隊在國際藥物化學(xué)領(lǐng)域頂級期刊《Journal of Medicinal Chemistry》以封面論文形式發(fā)表題為“Discovery of a Novel Small-Molecule Inhibitor Disrupting TRBP?Dicer Interaction against Hepatocellular Carcinoma via the Modulation of microRNA Biogenesis”的研究成果。該工作通過基于表型的高通量篩選發(fā)現(xiàn)一個苯基噁唑類小分子CIB-3b可以通過破壞TAR RNA結(jié)合蛋白2(transactivation response RNA-binding protein 2, TRBP)和Dicer的蛋白間相互作用,從而調(diào)控細(xì)胞內(nèi)微小RNA(microRNA, miRNA)的生物合成,有效的抑制肝癌細(xì)胞在體外和體內(nèi)的增殖與轉(zhuǎn)移。CIB-3b是國際上首個靶向TRBP-Dicer蛋白質(zhì)相互作用的化學(xué)小分子抑制劑,為開發(fā)針對miRNA治療肝癌提供了新的潛在治療手段。

封面論文
非編碼RNA占到了人體內(nèi)基因組中70%以上,被認(rèn)為是生命的暗物質(zhì)。這些非編碼RNA包含相當(dāng)多的種類,其中近年來被研究最多的是微小RNA與長鏈非編碼RNA。越來越多的證據(jù)表明,這些非編碼RNA參與了幾乎所有的生命過程,包括器官發(fā)育,組織修復(fù)以及免疫等活動。miRNAs是一種內(nèi)源性的、長度約為22個核苷酸的非編碼RNA,可與目標(biāo)mRNA結(jié)合從而影響其翻譯水平的表達(dá)。miRNAs表達(dá)水平失調(diào)是腫瘤的主要特征之一,這種異常會促進(jìn)癌細(xì)胞的增殖、遷移和轉(zhuǎn)移,維持腫瘤生長的微環(huán)境。目前若干個基于核酸的miRNA抑制劑或模擬物正在開展臨床研究,但是此類藥物開發(fā)存在較大的技術(shù)難度,包括脫靶效應(yīng)、較差的細(xì)胞通透性及非特異性激活免疫系統(tǒng)等。RNA結(jié)合蛋白(RNA-binding proteins)通過與不同類型的RNA結(jié)合,形成核糖核蛋白從而參與了對RNA代謝和功能的影響。雖然RNA結(jié)合蛋白參與了諸多疾病的發(fā)生,是潛在的新型藥物靶點(diǎn),但是目前由于篩選技術(shù)的限制,只發(fā)現(xiàn)了如HuR和LIN28等少數(shù)幾個RNA結(jié)合蛋白的化學(xué)小分子抑制劑。因此,進(jìn)一步采用基于表型的篩選方法,獲得RNA結(jié)合蛋白化學(xué)小分子抑制劑是針對非編碼RNA藥物開發(fā)的新途徑。
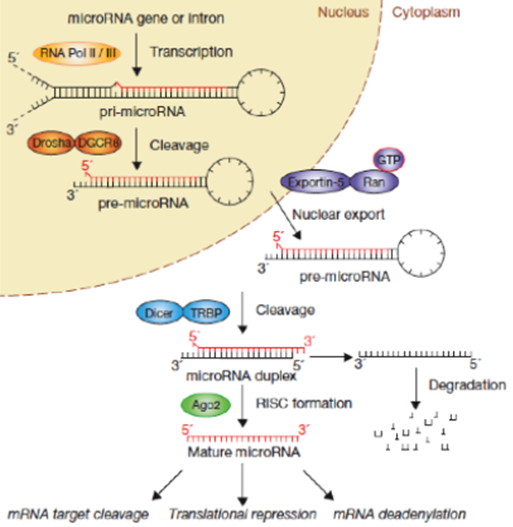
圖. microRNA的生物合成途徑
肝癌是全球第六大常見腫瘤,也是全球第三大癌癥相關(guān)死亡原因。其中,亞洲地區(qū)受飲食習(xí)慣和文化環(huán)境的影響,相比歐美國家發(fā)病率更高。2020年,中國肝癌患者占全球新發(fā)病例總數(shù)的45%,死亡病例占全球肝癌死亡總數(shù)的47%。手術(shù)切除是肝癌發(fā)病早期的一種治療方法,但治愈率并不理想,5年內(nèi)復(fù)發(fā)率高達(dá)70%。此外,由于肝癌早期的診斷難度較大,大多數(shù)患者確診時已經(jīng)是晚期;另一方面,高耐藥性和藥物毒性使得肝癌的藥物治療更加困難。因此,化療和靶向藥物如索拉菲尼和樂伐替尼的療效都不盡人意,中位總生存期僅為6-12個月。過去研究表明,miRNAs的種類和表達(dá)變化參與了肝癌發(fā)生的各個階段,也被作為生物標(biāo)志物用于癌癥早期診斷、預(yù)測治療效果和確認(rèn)進(jìn)展風(fēng)險。因此,通過化學(xué)小分子藥物調(diào)控肝癌細(xì)胞內(nèi)miRNA的表達(dá)將為肝癌治療提供新的治療手段。TRBP過去被發(fā)現(xiàn)作為一種RNA結(jié)合蛋白,參與到HIV的病毒復(fù)制,調(diào)控腫瘤轉(zhuǎn)移和血管生成密切相關(guān)基因mRNA的穩(wěn)定性。近年來的研究表明,TRBP也是miRNA加工過程中的關(guān)鍵蛋白,它能提高Dicer 剪切pre-miRNA形成成熟miRNA的效率和精度,而TRBP的突變將導(dǎo)致miRNA的異常表達(dá)而誘發(fā)癌癥的發(fā)生。2021年,王飛研究員團(tuán)隊同樣發(fā)表在《Journal of Medicinal Chemistry》(2021, 64:7404–7421)的文章中曾報道過,從中藥五味子中獲得的聯(lián)苯環(huán)辛烯類木脂素Gomisin M1通過靶向TRBP影響了細(xì)胞內(nèi)miRNA的生物合成從而抑制肝癌細(xì)胞的增殖和轉(zhuǎn)移,表明TRBP可以作為一個新的抗腫瘤藥物靶點(diǎn)。
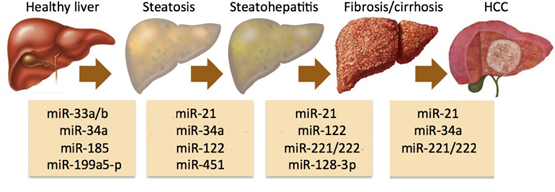
圖. microRNA參與了肝癌的發(fā)生與發(fā)展
本研究工作中,王飛研究員團(tuán)隊通過可以檢測細(xì)胞內(nèi)miRNA表達(dá)的高通量篩選及先導(dǎo)化合物結(jié)構(gòu)優(yōu)化,發(fā)現(xiàn)一個2-苯基噁唑衍生物CIB-3b能有效的抑制miRNA的生物合成(EC50 ~ 1.38 μM)。進(jìn)一步研究顯示,CIB-3b只影響了成熟miRNAs的表達(dá),而對miRNAs的前體包括primary-和precursor-miRNAs的表達(dá)沒有影響,并且在體外和動物體內(nèi)能顯著抑制肝癌細(xì)胞的增殖和轉(zhuǎn)移。通過對肝癌細(xì)胞miRNA表達(dá)譜和蛋白質(zhì)組的測序和分析發(fā)現(xiàn),CIB-3b影響了43個miRNAs的表達(dá),調(diào)控了Notch, TGF-β,EMT等與腫瘤增殖和轉(zhuǎn)移相關(guān)的信號通路。為了進(jìn)一步確定CIB-3b的直接靶點(diǎn),利用免疫共沉淀、間接競爭ELISA、基因敲除等研究方法,首次揭示了該化合物通過靶向TRBP,破壞了TRBP和Dicer的相互作用,進(jìn)而降低了Dicer剪切pre-miRNA的活性,從而影響了部分與腫瘤密切相關(guān)miRNAs的表達(dá)發(fā)揮其抗腫瘤作用。同時,利用核磁共振、表面等離子共振技術(shù)和等溫滴定等方法揭示了CIB-3b與TRBP具有直接的物理作用,其親和力KD ~為10 nM,遠(yuǎn)優(yōu)于報道的可以與TRBP結(jié)合的化學(xué)小分子Gomisin M1(KD ~ 8.06 μM)和依諾沙星(KD ~ 12.56 μM)。通過合成44個CIB-3b衍生物評估構(gòu)效關(guān)系,發(fā)現(xiàn)大部分化合物具有抑制miR-21的活性,其中有6個化合物與CIB-3b的活性相當(dāng),均表現(xiàn)出良好的抗腫瘤能力和靶向TRBP的親和力。蛋白質(zhì)-蛋白質(zhì)相互作用在調(diào)節(jié)生物過程,細(xì)胞和信號傳導(dǎo)途徑中起著至關(guān)重要的作用,因此靶向蛋白質(zhì)之間的界面在藥物發(fā)現(xiàn)中具有巨大的潛力。然而,靶向蛋白-蛋白相互作用長期以來被認(rèn)為是一項非常困難的任務(wù),因為界面相對較大,通常是扁平的而沒有特異性配體結(jié)合口袋。該研究首次發(fā)現(xiàn)了苯基噁唑衍生物可以通過破壞TRBP-Dicer蛋白相互作用,使細(xì)胞內(nèi)與腫瘤相關(guān)的miRNAs恢復(fù)到正常生理狀態(tài),為進(jìn)一步開發(fā)具有廣譜抗腫瘤作用的first-in-class創(chuàng)新藥物提供了新的藥物靶點(diǎn)及候選小分子。
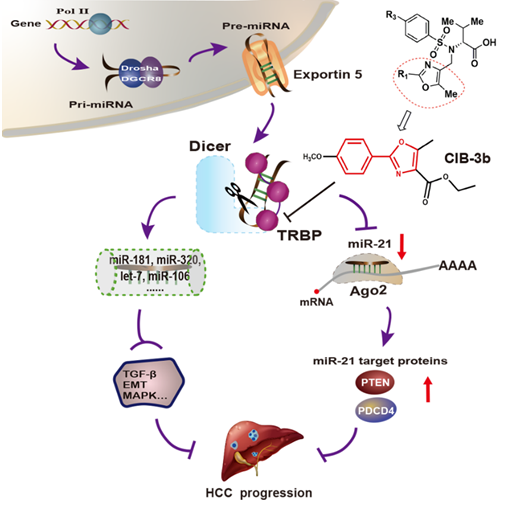
圖. CIB-3b的作用示意圖
中國科學(xué)院成都生物研究所天然產(chǎn)物結(jié)構(gòu)與功能項目組王飛研究員、張國林研究員、盧曉霞研究員,成都中醫(yī)藥大學(xué)胡凱峰教授為本論文共同通訊作者。該研究得到了國家自然科學(xué)基金和中國科學(xué)院戰(zhàn)略生物資源服務(wù)網(wǎng)絡(luò)計劃等項目的資助。




